Saphenion®: Faktencheck Venenkleber für Krampfadern – Anwendungserfahrungen an 4722 Stammkrampfadern
Saphenion®: Faktencheck Venenkleber für Krampfadern – von uns wird seit 10 Jahren in regelmäßiger Folge ein Faktencheck mit dem Ziel veröffentlicht, internationale Veröffentlichungen zum Thema mit eigenen Erfahrungen zu vergleichen und weiterhin aussagefähig zu bleiben. Auch unsere Patienten sind inzwischen sehr gut auch über dieses seit mehr als 13 Jahren aktiv praktizierte Therapieverfahren bei Stammkrampfadern informiert. Nach 155 Monaten Einsatz haben wir 2245 Patienten an 4722 Stammvenen therapiert – weltweit sind mittlerweile über 1 Million Patienten mit dem Venenkleber VenaSeal® behandelt worden.
Und aktuell in 2025 wurde eine Studie aus Japan veröffentlicht, diese bestätigt unsere Erfahrungen und Resultate in vollem Umfang!
Saphenion®: Faktencheck Venenkleber für Krampfadern – News der Fachgesellschaft Venenheilkunde
Die Deutsche Gesellschaft für Venenheilkunde (DGP) stellt in die aktuellen Leitlinien „S2k -Leitlinie zur Diagnostik und Therapie der Varicosis“ auch die Therapie mit dem Venenkleber VenaSeal® als Therapieempfehlung für die Therapie der Stammvaricosis ein.
Zusammen mit Kollegen aus München, Hildesheim, Köln, Düsseldorf, Rostock hat Saphenion® im Frühjahr 2020 anlässlich der „Bonner Venentage“ eine „VenaSeal® – Multicenter – Studie begonnen. Im November 2020 ist dann unsere gemeinsame „German Multicenter Study VenaSeal®“ veröffentlich worden.
Vor 155 Monaten haben wir mit dem Einsatz des Venenklebers bei der Therapie von Stammkrampfadern begonnen. Nunmehr stehen 4722 behandelte Venen im Op – Buch. Wir haben den Venenkleber bisher bei 2245 Patienten eingesetzt.
Neben vielen gut informierten Patienten, welche inzwischen diese Therapiemethode direkt nachfragen, haben auch gesetzliche Krankenkassen das – nicht mehr so neue – Verfahren in einigen Fällen anerkannt.
Saphenion®: Faktencheck Venenkleber für Krampfadern – 155 Monate Krampfadertherapie
Auch die meisten Privatversicherungen haben im Rahmen der vorgelegten Kostenvoranschläge die Therapieoption des Venenklebens von Krampfadern akzeptiert. Ebenso sind die Beihilfestellen des Bundes, der Länder Berlin / Brandenburg, Sachsen / Anhalt, Sachsen und Thüringen sowie Niedersachsen und Schleswig – Holstein nach Berichten unserer Patienten bereit, die Kosten für dieses in Europa 2011 zugelassene Therapieverfahren zu übernehmen.
Im Zweifel sollten unsere Patienten vor Vereinbarung eines Therapietermins eventuell mit ihrer Versicherung sprechen. In Einzelfällen werden vorgelegte Kostenvoranschläge zunächst ganz allgemein bestätigt, um dann nach der Therapie die Rechnung auf Basis alter Therapieverfahren in vielen Punkten in Frage zu stellen. So wird die in der ärztlichen Gebührenordnung GOÄ §6, Absatz 2 festgelegte Analogabrechnung für alle Katheterverfahren der modernen Krampfadertherapie unterlaufen!
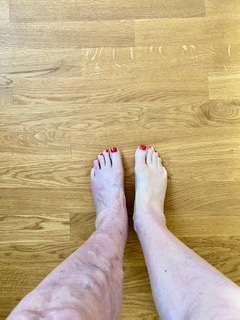
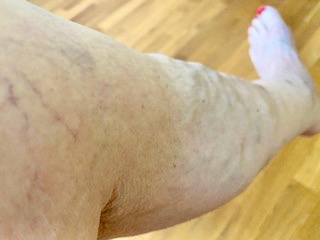
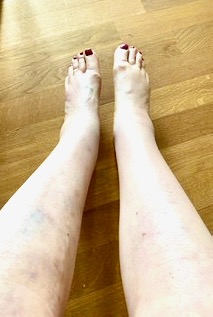
Saphenion®: Faktencheck Venenkleber bei Krampfadern – Eigene Fotodokumentation der Therapieergebnisse durch eine Patientin aus Berlin
Ein aktueller Fallbericht / Patienteninterview:
Saphenion® Gefäßzentrum Rostock – ein aktuelles Interview mit Frau Renate Schacht nach ihrer akuten Therapie mit dem Venenkleber VenaSeal® simultan an 2 duplexsonografisch festgestellten Stammkrampfadern. Die linke Stammkrampfader war in hohem Maße thrombosiert, der Thrombus reichte bis in die Beckenvene hinein – Wir führten neben der Verklebung der Venen auch eine Thrombusentfernung durch und Frau Schacht konnte dank Einsatz des Venenklebers auch simultan mit einer Thrombolysetherapie (Arixtra 7,5mg) behandelt werden.
Am 19. 05. 2025 erfolgte dann die Sanierung der komplett rekanalisierten Vena saphenas magna und der Vena saphena anterior am li. Bein nach der zuvor erlittenen kompletten OVT (oberflächigen Venenthrombose) der V. saphena magna und V. saphena anterior einschließlich der Magnacrosse und der V.iliaca externa.
Saphenion®: Faktencheck Venenkleber für Krampfadern – Internationale Ergebnisse
Diese werden bei der Literaturanalyse deutlich. Kollegen aus den USA, Korea und Holland, aus Russland und Hongkong haben 3 – 5 Jahres – Studien vorgelegt. Neben unserer eigenen 8 – Jahres – Langzeitstudie und der Deutschen VenaSeal® – Multicenter – Studie haben auch Morrisson et al. eine 5 – Jahres – Studie vorgelegt, ebenso Gibbson et al.. Die Ergebnisse sind in allen Studien nahezu identisch, die Verschlussrate nach diesen langen Zeiträumen liegt zwischen 94 – 97%.
Nach 155 Monaten praktischer Arbeit mit dem Venenkleber sehen wir – wie auch die internationalen Studien – die hohe Effektivität bei sehr geringer Nebenwirkungsrate. Zunächst vom Hersteller ausschließlich für normalkalibrige Stammvenen zugelassen und eingesetzt, hat sich der Kleber weitere Anwendungsbereiche der endovenösen Therapie erobert. So werden auch ektatische Venen und Aneurysmata inzwischen erfolgreich mittels Venenkleber therapiert.
Unsere Ergebnisse nach 155 Monaten Einsatz liegen bei 96,29% Verschlusseffektivität.
Damit ist der Venenkleber in der Effektivität besser im Vergleich zum etablierten Radiowellensystem – bei wesentlich weniger Nebenwirkungen und einer verkürzten post op. Erholungsphase.
Die Arbeitsfähigkeit ist am gleichen Tag ca. 3 Stunden nach der Therapie – oder bei Einsatz einer Sedierung – am darauf folgenden Tag wieder hergestellt.
Bontinis V, Bontinis A, Koutsoumpelis A, Chorti A, Rafailidis V, Giannopoulos A, Ktenidis K. A network meta-analysis on the efficacy and safety of thermal and nonthermal endovenous ablation treatments. J Vasc Surg Venous Lymphat Disord. 2023 Jul;11(4):854-865.e5. doi: 10.1016/j.jvsv.2023.03.011. Epub 2023 Apr 6. PMID: 37030442.
Gibson K, Morrison N, Kolluri R, Vasquez M, Weiss R, Cher D, Madsen M, Jones A. Twenty-four-month results from a randomized trial of cyanoacrylate closure versus radiofrequency ablation for the treatment of incompetent great saphenous veins. J Vasc Surg Venous Lymphat Disord. 2018 Sep;6(5):606-613. doi: 10.1016/j.jvsv.2018.04.009. Epub 2018 Jun 15. PubMed PMID: 29914814.
Imai T, Mo M, Hirokawa M, Kurihara N, Shokoku S, Sugiyama S, Shirasugi N, Kusagawa H, Hoshino Y, Yamamoto T, Hyodo E, Furubayashi K, Ogawa T. Mid-term results of cyanoacrylate closure for the treatment of incompetent great and small saphenous veins: Findings from a Japanese prospective consecutive multi-center registry: Mid-term results of cyanoacrylate closure. Phlebology. 2024 Aug 8:2683555241273013. doi: 10.1177/02683555241273013. Epub ahead of print. PMID: 39116289.
Lu PYJ, Fung CHC, Brooks C. Real-World Safety and Efficiency of Treating Symptomatic Varicose Veins with Endovenous Closure of Great, Small, and Anterior Accessory Veins Using Cyanoacrylate Glue (VenaSeal™): A Single-surgeon Multicenter Retrospective Study. Ann Vasc Surg. 2024 Dec 12;112:3-9. doi: 10.1016/j.avsg.2024.11.101. Epub ahead of print. PMID: 39672268.
Tang TY, Yap CJQ, Chan SL, Soon SXY, Yap HY, Lee SQW, Choke ETC, Chong TT. Early results of an Asian prospective multicenter VenaSeal real-world postmarket evaluation to investigate the efficacy and safety of cyanoacrylate endovenous ablation for varicose veins. J Vasc Surg Venous Lymphat Disord. 2021 Mar;9(2):335-345.e2. doi: 10.1016/j.jvsv.2020.03.020. Epub 2020 May 7. PMID: 32387378.
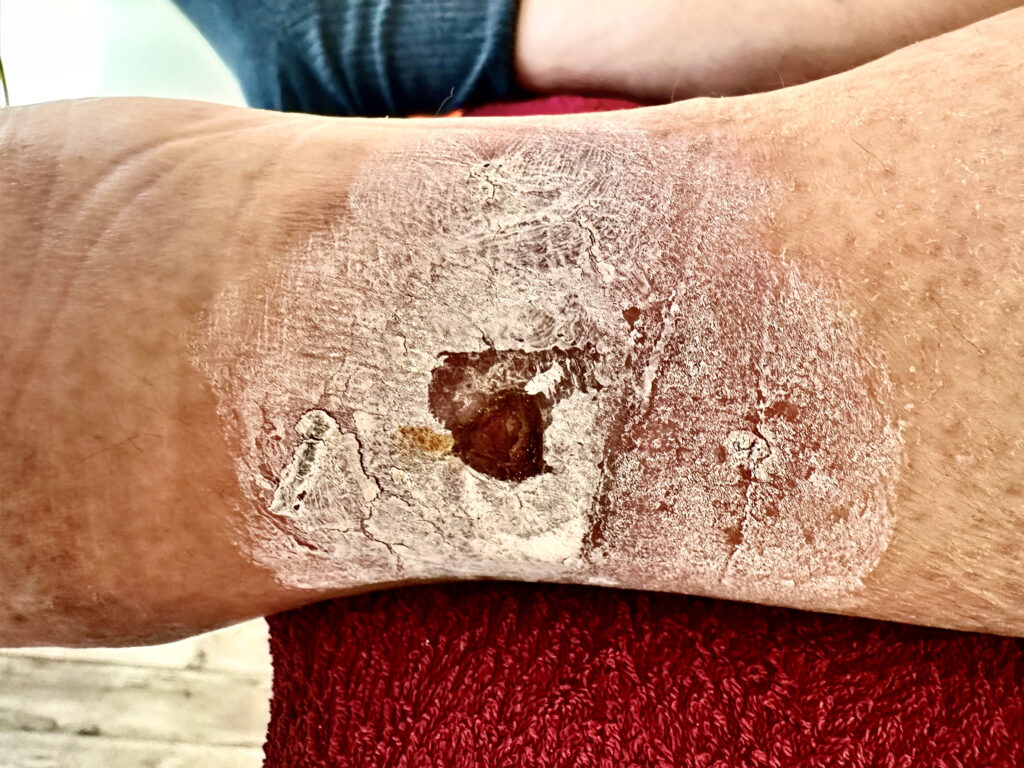
Saphenion®: Faktencheck Venenkleber für Krampfadern – Therapieerweiterungen Krampfadern – Verkleben beim Offenen Bein
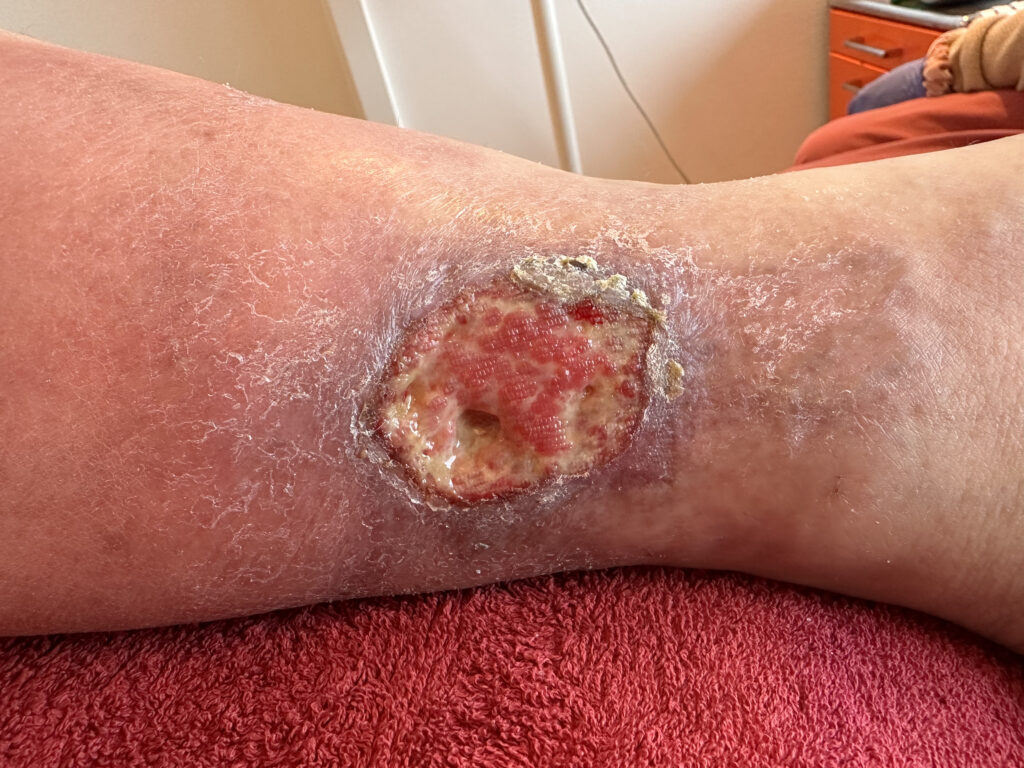
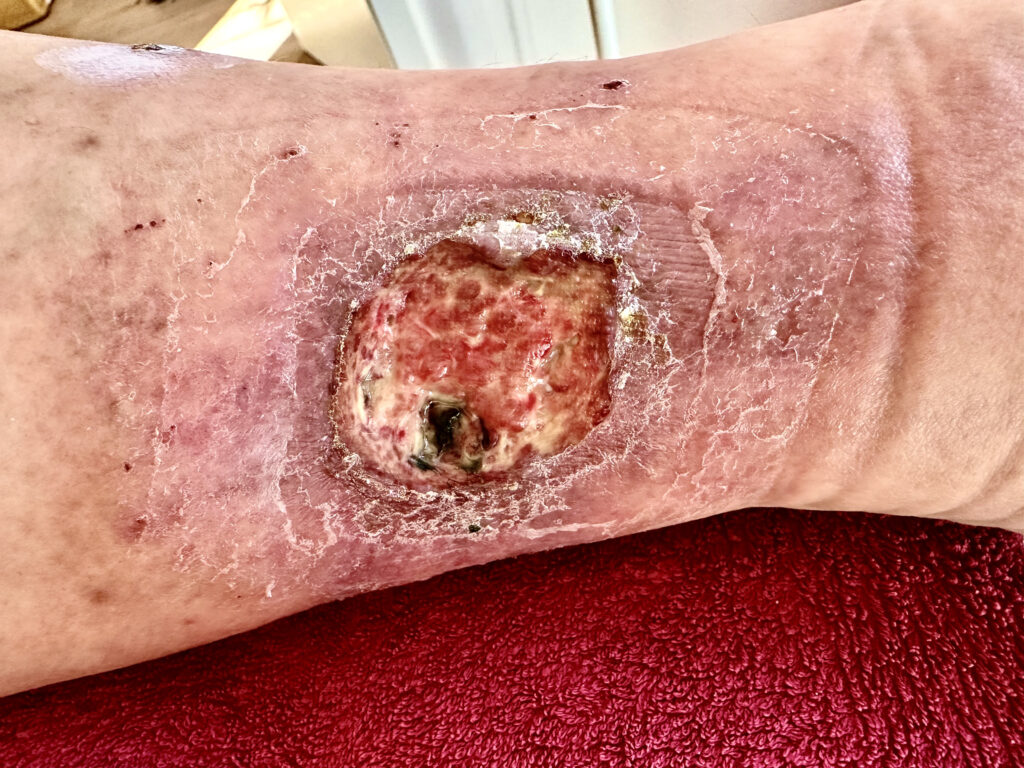
Die Behandlung des sog. „offenen Beines“ (Ulcus cruris) ist wesentlich einfacher, wirksamer und effektiver geworden. Der Venenkleber ist auch bei schwersten Befunden minimalinvasiv einsetzbar. Wir haben bisher bei unseren 78 Patienten mit Ulcus cruris den Venenkleber eingesetzt – mit sehr gutem Erfolg!
O’Banion LA, Reynolds KB, Kochubey M, Cutler B, Tefera EA, Dirks R, Kiguchi MM. Treatment of superficial venous reflux in CEAP 6 patients: a comparison of cyanoacrylate glue and radiofrequency ablation techniques. J Vasc Surg Venous Lymphat Disord. 2021 Jan 13:S2213-333X(21)00001-9. doi: 10.1016/j.jvsv.2020.12.082. Epub ahead of print. PMID: 33453440.
Park I. Successful use of VenaSeal system for treating large great saphenous vein of 2.84 cm diameter. Ann Surg Treat Res. 2018 Apr;94(4):219-221. doi: 10.4174/astr.2018.94.4.219. Epub 2018 Mar 26. PubMed PMID: 29629358; PubMed Central PMCID: PMC5880981.
Saphenion®: Faktencheck Venenkleber für Krampfadern – Verkleben von Perforanzvenen
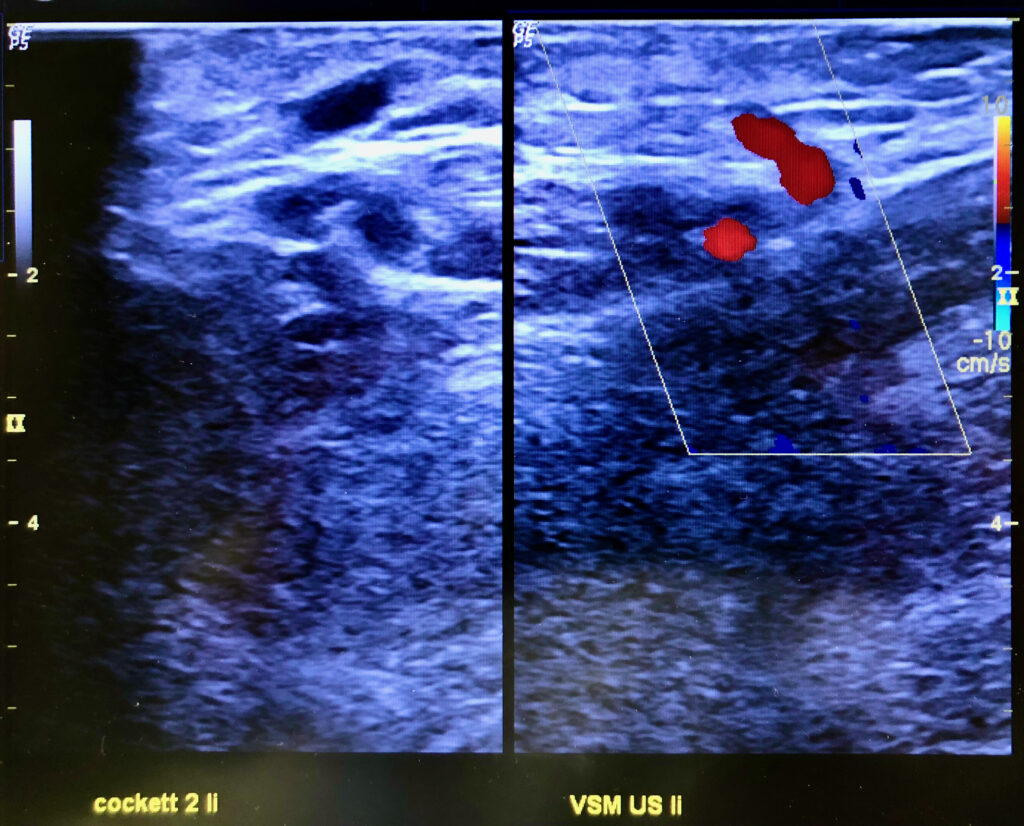
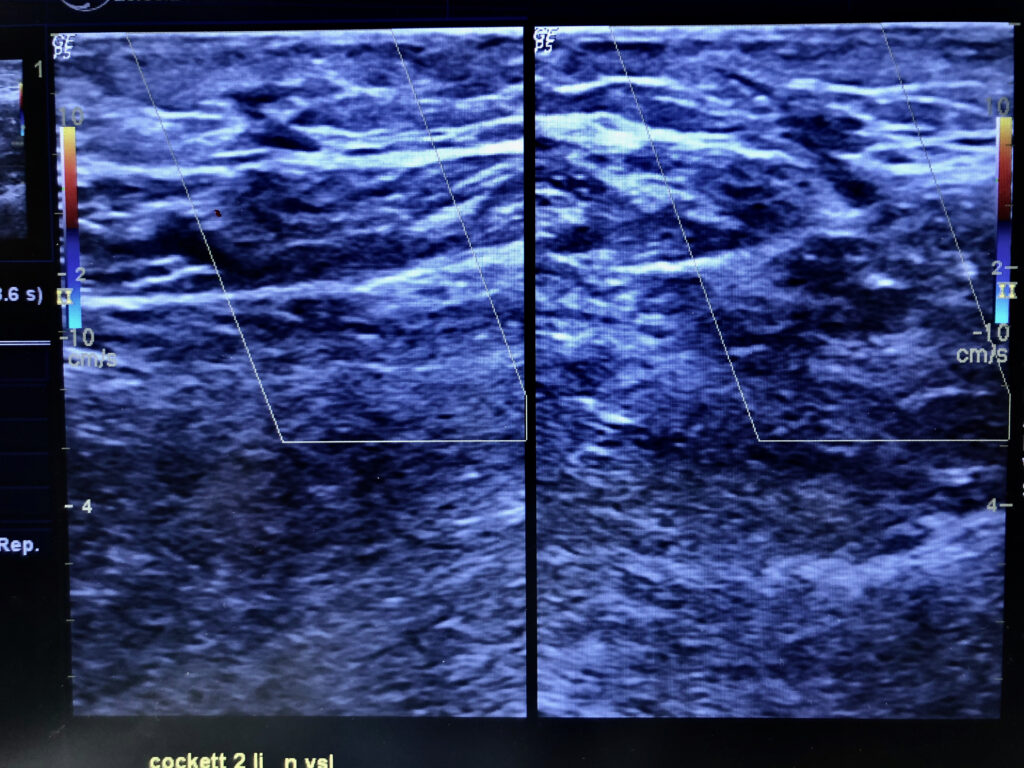
Das menschliche Venensystem hat etwa 140 Perforanz – Venenpaare, davon liegt die Mehrzahl am Unterschenkel. Von diesen Verbindungsvenen haben etwa 18 – 20 Venenpaare eine klinische Bedeutung. Deshalb werden sie auch Schlüsselperforanzvenen genannt. In über 60% der Fälle treten diese Venen als Paar auf und begleiten Hautarterien beim Durchtritt durch Muskelfaszien zur Haut.
Therapie von Perforanzkrampfadern mit Venenkleber: Diese Technik ergibt eine elegante und sichere Möglichkeit, die Perforanzvenen zeitgleich, zusammen mit der Therapie der Stammkrampfadern, mittels Venenkleber zu verschliessen. Zum Einen werden Perforanzvenen bereits beim Kathetermanöver in der Stammvene durch Abgabe eines zusätzlichen Klebertropfens an der Mündung (Ultraschallkontrolle!) verschlossen. Zum Anderen wird von uns nach Verklebung der Stammvenen in gleicher Sitzung mit der auf dem Op – Tisch liegenden Punktionsnadel auch die Perforanzvene direkt unter Sicht punktiert und verklebt.
Kiguchi MM, Reynolds KB, Cutler B, Tefera E, Kochubey M, Dirks R, Abramowitz SD, Woo EY, O’Banion LA. Perforator treatment is necessary after VenaSeal and ClosureFast endovenous saphenous vein closure in patients with CEAP 6. J Vasc Surg Venous Lymphat Disord. 2021 Jun 7:S2213-333X(21)00295-X. doi: 10.1016/j.jvsv.2021.04.020. Epub ahead of print. PMID: 34111593.
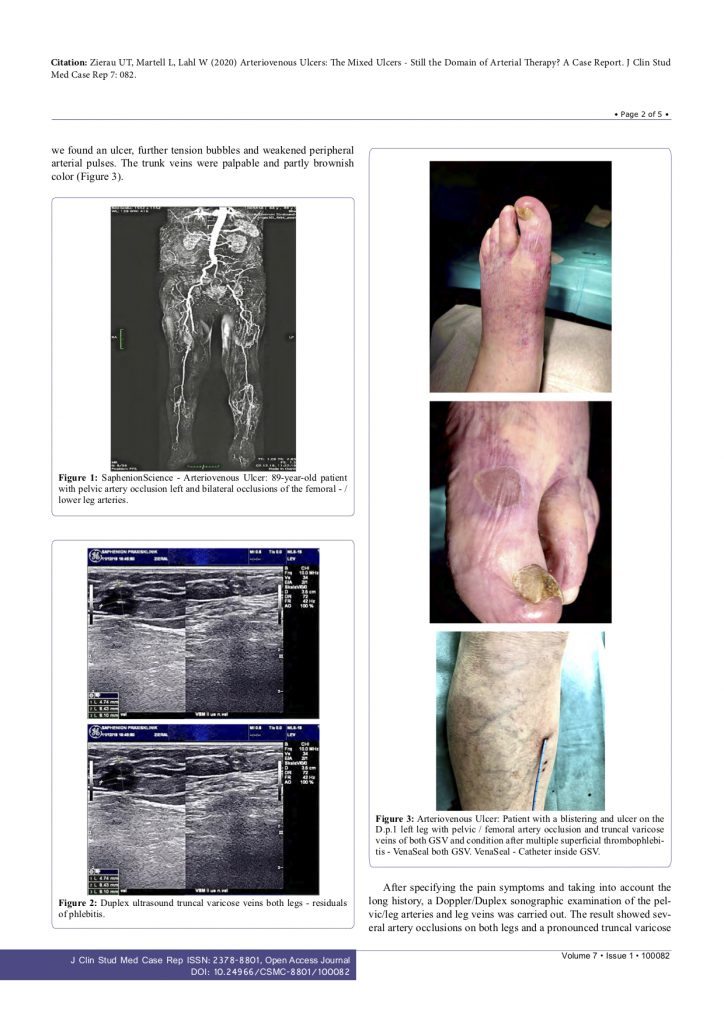
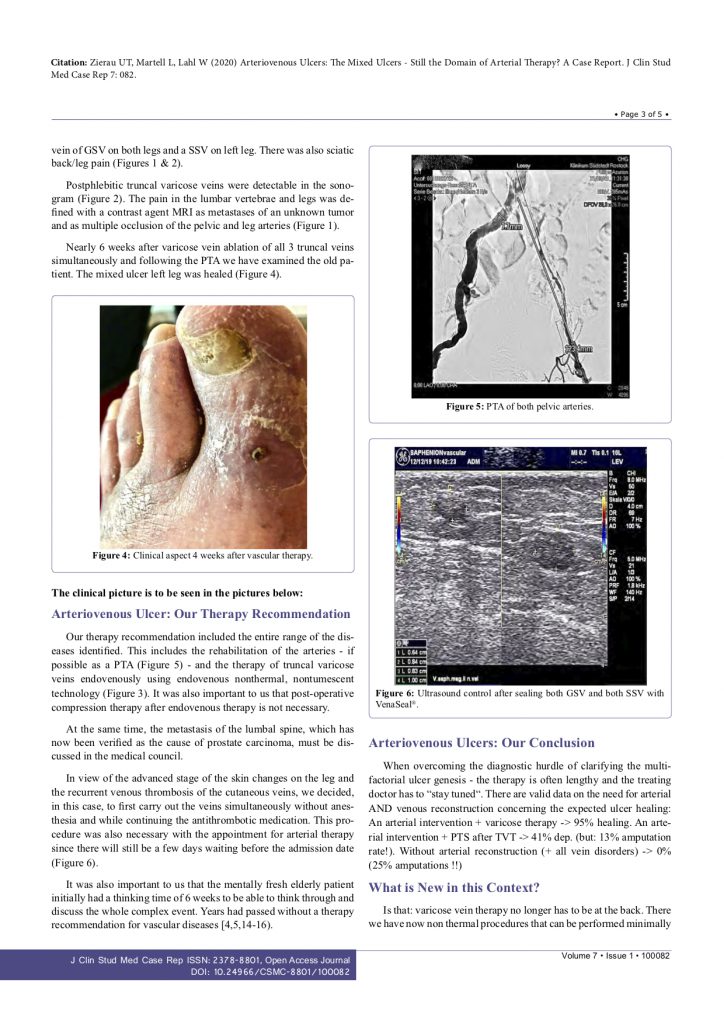
Saphenion®: Faktencheck Venenkleber für Krampfadern – Venentherapie beim Arterienverschluss
Saphenion® behandelt seit 7 Jahren auch Patienten, die an einer Arteriellen Verschlusskrankheit (Raucherbein) leiden und gleichzeitig auch funktionell defekte Stammkrampfadern haben, mittels VenaSeal® gleichzeitig – oder auch vor der Op an den Arterien – zunächst primär an den kranken Venen. Hiermit konnte nunmehr ein gewichtiges Dogma der Gefäßchirurgie – das Primat der Arterientherapie – aufgehoben werden!
Der therapeutische Grundsatz Kompressionsstrumpf nach der Krampfader – Op wird beim Kleber aufgehoben, somit können die geschädigten Arterien noch weiter Blut in die Beine pumpen!

Saphenion®: Faktencheck Venenkleber für Krampfadern – ambulante Therapie Schwerkranker
Wir behandeln inzwischen demenzkranke oder debile Patienten, Parkinson – / Epilepsie – Erkrankte und Trisomie – Patienten ambulant mit leichter Beruhigungsmedikation. Bei diesen Patienten haben wir in Rostock in der Vergangenheit mehrfach Kostenübernahmen der gesamten Therapiesumme auch durch Gesetzliche Krankenkassen erreichen können (AOK, Barmer,)
Auch systemische Infektionskrankheiten, wie Hepatitis, Covid – 19 oder HIV sind keine Kontraindikation – Patienten mit diesen Grunderkrankungen sind mehrfach erfolgreich mit dem Venenkleber therapiert worden – ohne Nebenwirkungen.
Multiallergische Erkrankungen sind ebenfalls keine Kontraindikationen für eine Behandlung mit dem Venenkleber.
Patienten mit lebenslanger Thrombose – / Embolietherapie sind ohne Absetzen oder Umstellen der dauerhaft notwendigen Antithrombose – Medikation ebenfalls erfolgreich ambulant zu behandeln.
Saphenion®: Faktencheck Venenkleber für Krampfadern: Interview mit Dr. Hans Modrow 5 Jahre nach der Venaseal® -Therapie
Saphenion®: Faktencheck Venenkleber für Krampfadern : Therapie beim Jugendlichen
In der Vergangenheit wurde die Krampfadertherapie bei Kindern und Jugendlichen sehr zurückhaltend praktiziert. Das bekannte radikalchirurgische „Stripping“ – Herausziehen der Stamm – und Seitenastkrampfadern – war in der Vorstellung der Gefäßchirurgen nun wirklich nicht geeignet, an Beinen von jungen Menschen primär zur Krampfadern – Therapie eingesetzt zu werden – wenn nicht ein akut lebensbedrohlicher Befund (Thrombose) oder eine Fehlbildung (Gefäßtumor) vorlag.

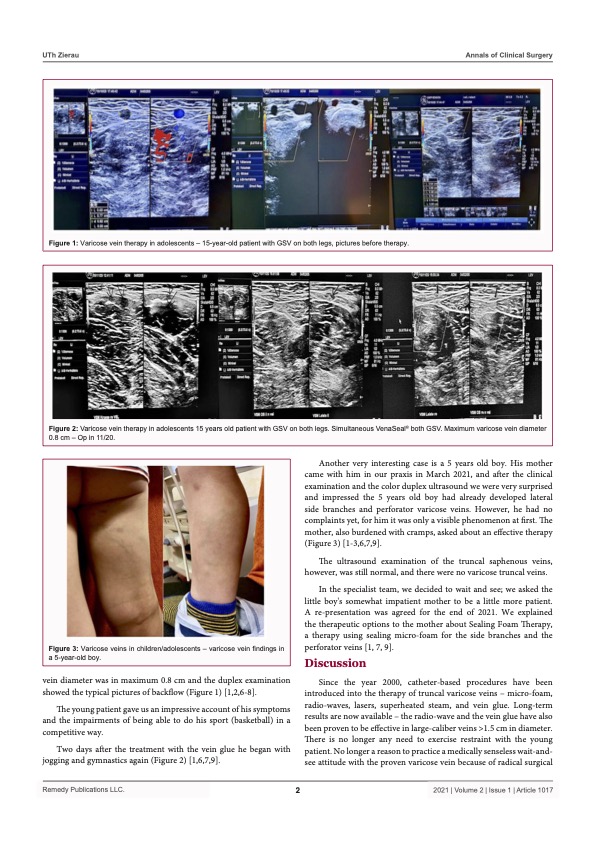

Seit dem Jahre 2000 sind kathetergestützte Verfahren in die Therapie der Stammvaricosis eingeführt worden – Mikroschaum, Radiowelle, Laser, Heißdampf, Venenkleber. Inzwischen liegen dafür Langzeitergebnisse vor – für die Radiowelle und den Venenkleber ist eine Effektivität auch bei kaliberstarken Venen > 1.5 cm Durchmesser nachgewiesen worden. Somit kein Grund mehr, Zurückhaltung beim jungen Patienten zu üben. Kein Gund mehr, wegen radikaler Op – Technik eine medizinisch sinnlose abwartenden Haltung bei der nachgewiesenen Stammkrampfader zu üben. Diese Krampfader heilt nicht mehr, nicht mit Creme, Gel oder Tablette und auch nicht mit Kompressionsstrumpf!
Ganz im Gegenteil bieten die Katheterverfahren gerade auch für die jugendliche Patientengruppe erhebliche Vorteile, wenn man an die Nebenwirkungen und Komplikationen radikaler chirurgischer Techniken denkt. Und ganz an das Ende der Therapiemöglichkeiten gedacht, sind die kalten „non thermischen“ Verfahren Venenkleber und Mikroschaum das Optimum für die Therapie von jungen Patienten. Keine Narkose, keine grossflächigen Anästhesie – Einspritzungen und beim VenaSeal® – Venenkleber auch kein Kompressionsstrumpf mehr. Und wir erreichen eine sofortige Mobilität für den jugendlichen Patienten.
Saphenion®: Faktencheck Venenkleber für Krampfadern: Therapie in der Schwangerschaft?
Die klassischen Therapiemethoden hierbei sind Kompressionstherapie mit Maßstrümpfen oder besser Strumpfhosen, manuelle Lymph – und Gewebemassagen und Wechselduschen, Kalte Güsse und viel Bewegung – hierzu wissen Hebammen und Geburtshelfer sehr gut Bescheid.
http://www.babycenter.de/a8586/krampfadern
Anders verhält es sich mit funktionell defekten Seitenästen und Stammkrampfadern. Diese Stammkrampfadern entwickeln sich im Übrigen nicht, wie von Netzvenen und Besenreisern bekannt, nach Entbindung und Abstillen weitgehend zurück! Hier drohen gerade auch in der Schwangerschaft (Hormone und mechanische Belastung) ernsthafte Komplikationen, wie Venenentzündungen oder gar Thrombosen.
Bisher galt das Dogma, dass während einer Schwangerschaft keine aktiven Therapiemethoden zur Behandlung der Stammvaricosis eingesetzt werden!
Die Venenentzündung wird mittels Kompressionstherapie, Gabe von – nicht durch die Plazenta in das ungeborene Kind hineinfließende – Antithrombosemedikamente und ggf. einem Absaugen des thrombosierten Blutes aus der entzündeten Vene behandelt. Unter Umständen macht sich hier jedoch unter prophylaktischen Aspekten auch eine aktive Therapie an den Stammkrampfadern nötig. Dies darf keine Narkose oder grossflächige Einspritzungen von Lokalanästhetika nach sich ziehen, da diese Medikamente via Plazenta auch den Fötus erreichen. Eine kleine Lokalanästhesie muss reichen! Herkömmliche radikalchirurgische Methoden entfallen gänzlich, die thermischen Verfahren Laser und Radiowelle sind ohne Vollnarkose oder Tumeszenzanästhesie nicht machbar, also kontraindiziert bei Schwangerschaft.
Seit 13 Jahren im klinischen Einsatz, steht uns heute das auch kathetergestützte Verfahren mit den notwendigen Kriterien auch für einen Einsatz in der Schwangerschaft zur Verfügung, das Venenkleben mittels VenaSeal® – Closure. Hierbei ist eine Anästhesie nicht mehr notwendig, der Kleber ist nach umfangreichen Prüfungen der amerikanischen Gesundheitsbehörde FDA nicht placentagängig und die Schwangere ist post op nach dem minimalinvasiven Kathetereingriff in keiner Weise immobilisiert.
Unter strenger Berücksichtigung der Indikationen zu diesem Eingriff – eine schwerwiegende Schmerzsymptomatik bei der Patientin, Venenentzündung und drohende Thrombose sowie schwere infektiöse Hautveränderungen und Ulcerationen – ist dieser kathetergestützte Eingriff mit dem Venenkleber nach umfassender Aufklärung und dem alleinigen Willen der Patientin durchführbar.
Saphenion®: Faktencheck Venenkleber für Krampfadern – Nebenwirkungen und Komplikationen
Eine aktuelle Suche in der internationalen Fachliteratur in Vorbereitung dieses updates hat in 4 Fällen (bei > 1 Million Patienten!) das Auftreten eine Kontaktdermatitis (Hautentzündung nach Kontakt mit Cyanoacrylat) und in erst einem Fall eine – vermeintliche – VenaSeal® – Allergie beschrieben. Weitere Komplikationen bei Anwendung oder im post op Verlauf werden nach wie vor nicht aufgezeigt. Eine VenaSeal® – Allergie haben wir nach therapierten 2245 Patienten und 4722 behandelten Venen noch nicht gesehen.
Unsere eigenen Erfahrungen zur fraglichen Allergie auf den Venenkleber wurden aktuell in einer internationalen Veröffentlichung dargestellt und bestätigt.
Watts TJ, Thursfield D, Haque R. Allergic contact dermatitis caused by VenaSeal tissue adhesive. Contact Dermatitis. 2019;80(6):393-395. doi:10.1111/cod. 13206
Jones AD, Boyle EM, Woltjer R, Jundt JP, Williams AN.J Vasc Surg Cases Innov Tech. 2019 Aug 7;5(3):372-374. doi: 10.1016/j.jvscit.2019.05.004. eCollection 2019 Sep.PMID: 31440717
Navarro-Triviño FJ, Cuenca-Manteca J, Ruiz-Villaverde R. Allergic contact dermatitis with systemic symptoms caused by VenaSeal. Contact Dermatitis. 2020;82(3):185-187. doi:10.1111/cod. 13431
Fiengo L, Gwozdz A, Tincknell L, Harvey V, Watts T, Black S. VenaSeal closure despite the allergic reaction to n-butyl cyanoacrylate. J Vasc Surg Cases Innov Tech. 2020;6(2):269-271. Published 2020 Apr 10. doi:10.1016/j.jvscit.2020.034

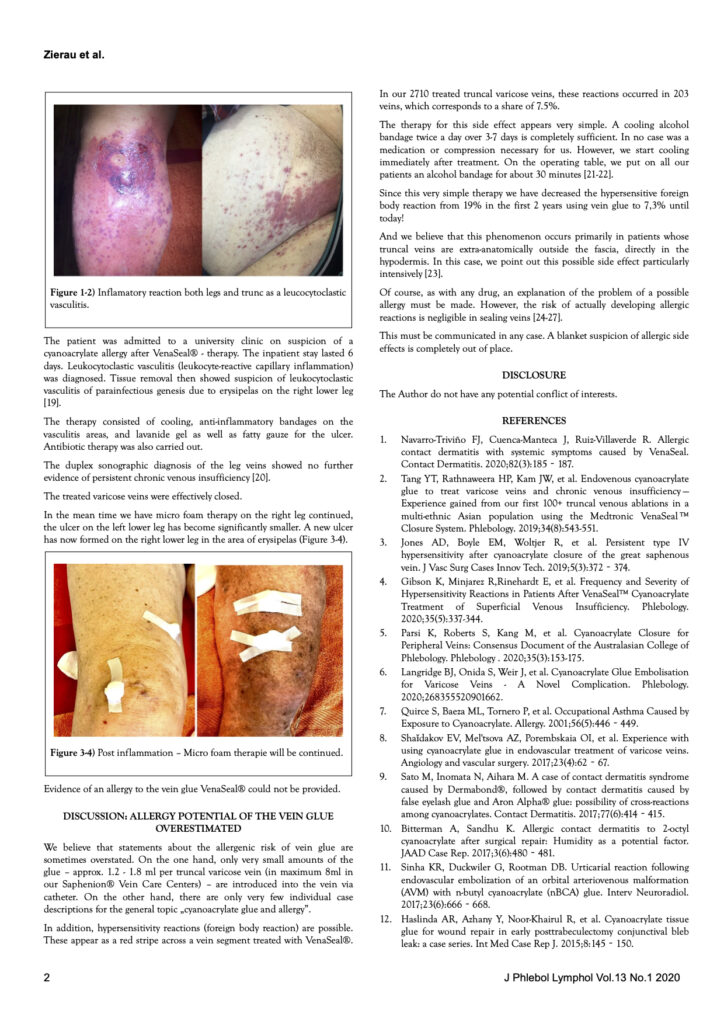

Und auch unsere mehrfach veröffentlichte und vorgetragene Aussage zur vermeintlichen Venenentzündung nach dem Venenkleber – es ist eine immunologische Gewebereaktion des umliegenden Gewebes – wurden inzwischen ebenfalls vielfach in weiteren wissenschaftlichen Arbeiten bestätigt:
Gibson K, Minjarez R, Rinehardt E, Ferris B. Frequency and severity of hypersensitivity reactions in patients after VenaSeal™ cyanoacrylate treatment of superficial venous insufficiency. Phlebology. 2020;35(5):337-344. doi:10.1177/0268355519878618
Nasser H, Ivanics T, Shakaroun D, Lin J. Severe phlebitis-like abnormal reaction following great saphenous vein cyanoacrylate closure. J Vasc Surg Venous Lymphat Disord. 2019 Jul;7(4):578-582. doi: 10.1016/j.jvsv.2019.03.010. Epub 2019 May 8. PubMed PMID: 31078516.
Tang TY, Tiwari A. The VenaSeal™ Abnormal Red Skin Reaction: Looks Like but is not Phlebitis!. Eur J Vasc Endovasc Surg. 2018;55(6):841. doi:10.1016/j.ejvs.2018.02.003
Park I, Jeong MH, Park CJ, Park WI, Park DW, Joh JH. Clinical Features and Management of „Phlebitis-like Abnormal Reaction“ After Cyanoacrylate Closure for the Treatment of Incompetent Saphenous Veins. Ann Vasc Surg. 2019;55:239-245. doi:10.1016/j.avsg.2018.07.040
Park I. Human Saphenous Vein Histopathology 2 Years After Cyanoacrylate Closure Using the VenaSeal™ System. Ann Vasc Surg. 2021 Feb;71:534.e17-534.e21. doi: 10.1016/j.avsg.2020.09.017. Epub 2020 Sep 16. PMID: 32949737.
In einer grossen amerikanischen Meta-Analyse wurden alle auch von uns bisher publizierten und in unseren News dargestellten Ergebnisse und Erfahrungen zur VenaSeal® – Therapie bestätigt:
Kolluri R, Chung J, Kim S, Nath N, Bhalla BB, Jain T, Zygmunt J, Davies A. Network meta-analysis to compare VenaSeal with other superficial venous therapies for chronic venous insufficiency. J Vasc Surg Venous Lymphat Disord. 2020 Feb 13. pii: S2213-333X(19)30702-4. doi: 10.1016/j.jvsv.2019.12.061. [Epub ahead of print] Review. PubMed PMID: 32063522.
Unser Leserbrief an die Zeitschrift „Phebologie“


Ein weiterer Leserbrief von unserem Kollegen Prof. Richard Brandl aus München:



Saphenion®: Faktencheck Venenkleber für Krampfadern – Gespräch mit Prof. Dr. med. Thomas Bürger, Vorsitzender der Leitlinienkomission der Deutschen Gesellschaft für Gefäßchirurgie, über das VenaSeal® – Verfahren
Saphenion®: Faktencheck Venenkleber für Krampfadern – Unsere Meinung
Anhand unserer fast 13 – jährigen praktischen Erfahrungen an inzwischen 4722 therapierten Krampfadern bei 2245 Patienten möchten wir aus unserer klinisch – fachlichen Sicht für den Faktencheck bestätigen:
Der Venenkleber ist uneingeschränkt biokompatibel, wir haben bisher, nach 155 Monaten Anwendung, keine Allergie gesehen. Es finden sich in der Literatur vier Arbeiten, die eine Kontaktallergie der Haut nach Berühren des Klebers beschreiben. Fragliche Allergien nach Injektion in die Stammkrampfadern sind bisher weltweit erst in zwei Fällen beschrieben.
Die Nebenwirkungsrate liegt demzufolge deutlich unter der vergleichbarer thermischer endovenöser Techniken (Laser, Radiowelle) bei der Behandlung der Stammvaricosis.
Und der Venenkleber ist nach einer Reihe kontrollierter Studien die Therapie mit der grössten Patientenzufriedenheit – wie dies auch ganz aktuell im unten angehängten Artikel eindrucksvoll bestätigt wird.
Lu PYJ, Fung CHC, Brooks C. Real-World Safety and Efficiency of Treating Symptomatic Varicose Veins with Endovenous Closure of Great, Small, and Anterior Accessory Veins Using Cyanoacrylate Glue (VenaSeal™): A Single-surgeon Multicenter Retrospective Study. Ann Vasc Surg. 2025 Mar;112:3-9. doi: 10.1016/j.avsg.2024.11.101. Epub 2024 Dec 12. PMID: 39672268.
Watts TJ, Thursfield D, Haque R. Allergic contact dermatitis caused by VenaSeal tissue adhesive. Contact Dermatitis. 2019 Jun;80(6):393-395. doi 10.1111/cod.13206. Epub 2019 Jan 30. PubMed PMID: 30582174.
Die Bioresorption des Klebers dauert zwischen 12 – 24 Monate. Es zeigen sich auch beim Menschen die gleichen Resorptionsprozesse wie in den inzwischen über 153 Veröffentlichungen zur Bioresorption beim Tier. Die Resorptionsmodelle im Tierversuch zeigen sämtlich einen biologischen Abbau des Cyanoacrylat – Klebers zwischen 4 und 9 Monaten. Die Resorption des Klebers ist bei regelmäßigen Ultraschallkontrollen auch makroskopisch zu verfolgen.
Aber nicht nur das ist interessant: Inzwischen liegen uns eigene histologische Befunde von menschlichen Venen 10 – 14 Monate nach endovenöser Cyanoacrylat – Verklebung mit dem VenaSeal® System vor. Diese zeigen in allen vier nachuntersuchten Fällen einen kompletten Abbau des Klebers in den Resten der Vene. Und auch hier gibt es neben unseren eigenen Ergebnissen inzwischen eine weitere Veröffentlichung:
Almeida JI, Murray SP, Romero ME. Saphenous vein histopathology 5.5 years after cyanoacrylate closure. J Vasc Surg Venous Lymphat Disord. 2019 Jul 4. pii: S2213-333X(19)30325-7. doi: 10.1016/j.jvsv.2019.04.014. [Epub ahead of print] PubMed PMID: 31281102.
Saphenion®: Faktencheck Venenkleber für Krampfadern – Therapie an Unterschenkelvenen, Rezidivgefahr
Am Unterschenkel ist die thermische Therapie (Laser, Radiowelle, Heissdampf) inzwischen international und auch national in ein kritisches Licht gerückt, da die Zahl der Nervenläsionen nach thermischer Therapie nicht zu vernachlässigen ist.
Auf der Jahrestagungen der Deutschen Gesellschaft für Venenheilkunde in 2022, 2023 und 2024 wurde dieses Thema erneut kontrovers diskutiert. Im Resultat wurde in Mehrheit kritisch Stellung bezogen zur thermischen Therapie an der Vena saphena parva und der V. saphena magna am Unterschenkel sowie der Therapie von Perforanzvenen mittels Laser oder Radiowelle. Auch bei der Therapie von Rezidivkrampfadern nach radikalchirurgischer Stripping – Op gelten inzwischen diese Vorbehalte.
Hier empfehlen viele Kollegen jetzt einen Verzicht auf die thermischen Verfahren Laser und Radiowelle, alternativ sind die kathetergestützte Mikroschaumtherapie oder eben der Venenkleber VenaSeal® oder VenaBlock® möglich. Nach unseren Erfahrungen, basierend auf einer eigenen Studie an über 2000 Patienten, haben wir für uns eine Indikation für Mikroschaum oder VenaSeal® definiert. Wir behandeln Stammvenen am Unterschenkel mit einem Durchmesser bis zu 0,50 cm mittels Mikroschaum, Stammvenen mit einem größeren Durchmesser werden mittels Venenkleber therapiert.
Damit entfällt auch unsere Alternativempfehlung Radiowelle für die Stammvenen am Unterschenkel, wie wir sie bisher in unseren Aufklärungsgesprächen ausgesprochen haben. Am Unterschenkel behandeln wir jetzt ausschließlich mit nonthermischen Verfahren!
Dieses Vorgehen wurde aktuell ebenfalls in den „Aktuellen Leitlinien zur Therapie der Varicosis“ der DGP verankert:

Das radikale Stripping ist aus unserer Sicht am Unterschenkel überhaupt nicht mehr indiziert.
Saphenion®: Faktencheck Venenkleber für Krampfadern – Besenreiser und Netzvenen?
Der Venenkleber für Krampfadern ist nicht – wie hier und da zu lesen und auch angefragt – für die Therapie von kosmetisch störenden Netzvenen und Besenreisern geeignet. Dazu steht der seit 2010 als „Goldstandard“ geltende Mikroschaum als Kombinationstherapie zur Verfügung.
Eine simultane Doppeltherapie mit Mikroschaum (Ethoxysklerol) ist möglich, birgt aber die Gefahr von Venenentzündungen in sich. Wissenschaftliche Studien zu dieser Kombinationstherapie haben Gibson et al. vorgelegt. Wichtig ist, zunächst die Abheilung der Stammkrampfader abzuwarten – in vielen Fällen kommt es zu einem deutlichen Rückgang der Seitenastvaricosis! Auch bei Saphenion® wird dieser Fakt berücksichtigt und wir führen notwendige Mikroschaumtherapien erst 14 – 21 Tage nach der VenaSeal® – Therapie durch.
Saphenion®: Faktencheck Venenkleber für Krampfadern – Das Trio infernale der Zöllner bei uns zum Wartezimmerkonzert
Photos / Videos: Sylvia Gippe, Claudia, Utzius
Papers / Links:
Kopie von Seite 11 des FDA – Approvals zur Biokompatibilität des VenaSeal® – Venenklebers:
Table 4: Results of Biocompatibility Testing – VenaSeal Adhesive (Polymerized and the Unpolymerized States) Test Method Reference Results Cytotoxicity (Elution Method) ISO 10993-5.
The cumulative results of the VenaSeal adhesive material cytotoxicity testing, in combination with assessments of toxicological risk and in vivo use, support an overall favorable cytotoxicity profile for the VenaSeal adhesive material per its intended use.
ISO Maximization Sensitization Study(Guinea Pigs)ISO 10993-10VenaSeal adhesive does not elicit a sensitization response
ISO Intracutaneous Reactivity – ISO 10993-10: The cumulative results support that the VenaSeal® adhesive material does not cause intracutaneous reactivity (Material Mediated Rabbit Pyrogenicity
ISO 10993-5US Pharmacopeia Section 151: The cumulative results support that the VenaSeal adhesive material is non-pyrogenic.
Acute Systemic Toxicity- ISO 10993-11: The cumulative results support that the VenaSeal adhesive material is not considered to cause acute systemic toxicity
Subacute / Subchronic ToxicityImplantation (13 weeks) – ISO 10993-11 / ISO 10993-6: The cumulative results support that the VenaSeal adhesive material does not result in any specific adverse systemic toxicological findings in the tissues examined Genotoxicity (Bacterial Mutagenicity, in vitro Mouse Lymphoma Assay, Mouse Micronucleus Assay)
ISO 10993-3: The cumulative results support that the VenaSeal adhesive material is non-mutagenic Hemo-compatibility (Hemolysis, Complement Activation, Partial Thromboplastin Time, Platelet and Leukocyte Count), ASTM F-756-08
ISO 10993-4: The cumulative results support that the VenaSeal adhesive material is non-hemolytic and not chronic toxicity Implantation (26 Weeks)
ISO 10993-11/ ISO 10993-6: The cumulative results support that VenaSeal adhesive does not cause any significant adverse systemic or local toxicity in the tissues examined.
Quelle: Summary – Food and Drug Administration / FDA
Almeida JI, Murray SP, Romero ME. Saphenous vein histopathology 5.5 years after cyanoacrylate closure. J Vasc Surg Venous Lymphat Disord. 2020 Mar;8(2):280-284. doi: 10.1016/j.jvsv.2019.04.014. Epub 2019 Jul 4. PubMed PMID: 31281102.
Bahi M, Guazzo L, Taumoepeau L. Real-world short-term VenaSeal ablation outcomes for symptomatic saphenous incompetence. Vascular. 2023 Jun;31(3):521-525. doi: 10.1177/17085381221077511. Epub 2022 Feb 25. PMID: 35209758.
Bontinis V, Bontinis A, Koutsoumpelis A, Chorti A, Rafailidis V, Giannopoulos A, Ktenidis K. A network meta-analysis on the efficacy and safety of thermal and nonthermal endovenous ablation treatments. J Vasc Surg Venous Lymphat Disord. 2023 Jul;11(4):854-865.e5. doi: 10.1016/j.jvsv.2023.03.011. Epub 2023 Apr 6. PMID: 37030442.
Bozkurt AK, Balkanay OO, Dinc R. Comparative analysis of VenaBlock and VenaSeal Systems for catheter-guided endovenous cyanoacrylate closure in treating chronic venous insufficiency of the lower extremity: effectiveness and feasibility. Int Angiol. 2024 Jun;43(3):331-341. doi: 10.23736/S0392-9590.24.05143-5. Epub 2024 Jul 23. PMID: 39041783.
Chan YC, Law Y, Cheung GC, Ting AC, Cheng SW. Cyanoacrylate glue used to treat great saphenous reflux: Measures of the outcome. Phlebology. 2017 Mar;32(2):99-106. doi 10.1177/0268355516638200. Epub 2016 Jul 9. PubMed PMID: 27052039.
Chan SSJ, Yap CJQ, Tan SG, Choke ETC, Chong TT, Tang TY. The utility of endovenous cyanoacrylate glue ablation for incompetent saphenous veins in the setting of venous leg ulcers. J Vasc Surg Venous Lymphat Disord. 2020 Mar 20. PII: S2213-333X(20)30100-1. doi: 10.1016/j.jvsv.2020.01.013. [Epub ahead of print] PubMed PMID: 32205130.
Cho S, Park HS, Lee T, Byun SJ, Yun WS, Yang SS, Kim H, Kim WS, Joh JH, Jung IM. CASS (CyanoAcrylate closure versus Surgical Stripping for incompetent saphenous veins) study is a randomized controlled trial comparing clinical outcomes after cyanoacrylate closure and surgical stripping for treating incompetent saphenous veins. Trials. 2020 Jun 3;21(1):460. doi 10.1186/s13063-020-04393-0. PMID: 32493398; PMCID: PMC7268719.
Comby PO, Guillen K, Chevallier O, Lenfant M, Pellegrinelli J, Falvo N, Midulla M, Loffroy R. Endovascular Use of Cyanoacrylate-Lipiodol Mixture for Peripheral Embolization: Properties, Techniques, Pitfalls, and Applications. J Clin Med. 2021 Sep 23;10(19):4320. doi: 10.3390/jcm10194320. PMID: 34640339; PMCID: PMC8509239.
Dinc R. VenaBlock® and VenaSeal® class III cyanoacrylate products are effective and safe in varicose vein treatment. Phlebology. 2024 May;39(4):284-285. doi: 10.1177/02683555231221319. Epub 2023 Dec 10. Erratum in: Phlebology. 2024 Dec;39(10):723. doi: 10.1177/02683555241264093. PMID: 38073234.
García-Carpintero E, Carmona M, Chalco-Orrego JP, González-Enríquez J, Imaz-Iglesia I. Systematic review and meta-analysis of endovenous cyanoacrylate adhesive ablation for incompetent saphenous veins. J Vasc Surg Venous Lymphat Disord. 2020 Mar;8(2):287-296. doi: 10.1016/j.jvsv.2019.09.010. Epub 2020 Jan 6. PMID: 31917181.
Gibson K, Ferris B. Cyanoacrylate closure of incompetent great, small, and accessory saphenous veins without post-procedure compression: Initial outcomes of a post-market evaluation of the VenaSeal System (the WAVES Study). Vascular. 2017 Apr;25(2):149-156. doi 10.1177/1708538116651014. Epub 2016 Jul 9. PubMed PMID: 27206470.
Gibson K, Morrison N, Kolluri R, Vasquez M, Weiss R, Cher D, Madsen M, Jones A. Twenty-four month results from a randomized trial of cyanoacrylate closure versus radiofrequency ablation for the treatment of incompetent great saphenous veins. J Vasc Surg Venous Lymphat Disord. 2018 Sep;6(5):606-613. doi: 10.1016/j.jvsv.2018.04.009. Epub 2018 Jun 15. PubMed PMID: 29914814.
Gloviczki P, Lawrence PF, Wasan SM, Meissner MH, Almeida J, Brown KR, Bush RL, Di Iorio M, Fish J, Fukaya E, Gloviczki ML, Hingorani A, Jayaraj A, Kolluri R, Murad MH, Obi AT, Ozsvath KJ, Singh MJ, Vayuvegula S, Welch HJ. The 2023 Society for Vascular Surgery, American Venous Forum, and American Vein and Lymphatic Society clinical practice guidelines for managing varicose veins of the lower extremities. Part II: Endorsed by the Society of Interventional Radiology and the Society for Vascular Medicine. J Vasc Surg Venous Lymphat Disord. 2024 Jan;12(1):101670. doi: 10.1016/j.jvsv.2023.08.011. Epub 2023 Aug 29. Erratum in: J Vasc Surg Venous Lymphat Disord. 2024 Sep;12(5):101923. doi: 10.1016/j.jvsv.2024.101923. PMID: 37652254; PMCID: PMC11523430.
Imai T, Mo M, Hirokawa M, Kurihara N, Shokoku S, Sugiyama S, Shirasugi N, Kusagawa H, Hoshino Y, Yamamoto T, Hyodo E, Furubayashi K, Ogawa T. Mid-term results of cyanoacrylate closure for the treatment of incompetent great and small saphenous veins: Findings from a Japanese prospective consecutive multi-center registry: Mid-term results of cyanoacrylate closure. Phlebology. 2024 Aug 8:2683555241273013. doi: 10.1177/02683555241273013. Epub ahead of print. PMID: 39116289.
Jones AD, Boyle EM, Woltjer R, Jundt JP, Williams AN.J Vasc Surg Cases Innov Tech. 2019 Aug 7;5(3):372-374. doi: 10.1016/j.jvscit.2019.05.004. eCollection 2019 Sep.PMID: 31440717
Jones AD, Boyle EM, Woltjer R, Jundt JP, Williams AN. Persistent type IV hypersensitivity after cyanoacrylate closure of the great saphenous vein. J Vasc Surg Cases Innov Tech. 2019 Aug 7;5(3):372-374. doi: 10.1016/j.jvscit.2019.05.004. eCollection 2019 Sep. PubMed PMID: 31440717; PubMed Central PMCID: PMC6699189.
Kiguchi MM, Reynolds KB, Cutler B, Tefera E, Kochubey M, Dirks R, Abramowitz SD, Woo EY, O’Banion LA. Perforator treatment is needed after VenaSeal and ClosureFast endovenous saphenous vein closure in CEAP 6 patients. J Vasc Surg Venous Lymphat Disord. 2021 Jun 7:S2213-333X(21)00295-X. doi: 10.1016/j.jvsv.2021.04.020. Epub ahead of print. PMID: 34111593.
Kolluri R, Chung J, Kim S, Nath N, Bhalla BB, Jain T, Zygmunt J, Davies A. Network meta-analysis to compare VenaSeal with other superficial venous therapies for chronic venous insufficiency. J Vasc Surg Venous Lymphat Disord. 2020 Feb 13. PII: S2213-333X(19)30702-4. doi: 10.1016/j.jvsv.2019.12.061. [Epub ahead of print] Review. PubMed PMID: 32063522.
Lu PYJ, Fung CHC, Brooks C. Real-World Safety and Efficiency of Treating Symptomatic Varicose Veins with Endovenous Closure of Great, Small, and Anterior Accessory Veins Using Cyanoacrylate Glue (VenaSeal™): A Single-surgeon Multicenter Retrospective Study. Ann Vasc Surg. 2025 Mar;112:3-9. doi: 10.1016/j.avsg.2024.11.101. Epub 2024 Dec 12. PMID: 39672268.
Nasser H, Ivanics T, Shakaroun D, Lin J. Severe phlebitis-like abnormal reaction following great saphenous vein cyanoacrylate closure. J Vasc Surg Venous Lymphat Disord. 2019 Jul;7(4):578-582. doi: 10.1016/j.jvsv.2019.03.010. Epub 2019 May 8. PubMed PMID: 31078516.
Navarro-Triviño FJ, Cuenca-Manteca J, Ruiz-Villaverde R. Allergic contact dermatitis with systemic symptoms caused by VenaSeal. Contact Dermatitis. 2020 Mar;82(3):185-187. doi 10.1111/cod.13431. Epub 2019 Nov 15. PubMed PMID: 31674037.
Park I. Successful use of VenaSeal system for the treatment of large great saphenous vein of 2.84 cm diameter. Ann Surg Treat Res. 2018 Apr;94(4):219-221. doi: 10.4174/astr.2018.94.4.219. Epub 2018 Mar 26. PubMed PMID: 29629358; PubMed Central PMCID: PMC5880981.
Park I. Initial Outcomes of Cyanoacrylate Closure, VenaSeal System, for treating the Incompetent Great and Small Saphenous Veins. Vasc Endovascular Surg. 2017 Nov;51(8):545-549. doi 10.1177/1538574417729272. Epub 2017 Oct 2. PubMed PMID: 28969499.
Park I, Kim D. Correlation Between the Immediate Remnant Stump Length and Vein Diameter After Cyanoacrylate Closure Using the VenaSeal System During Treatment of an Incompetent Great Saphenous Vein. Vasc Endovascular Surg. 2019 Oct 3:1538574419879563. doi:10.1177/1538574419879563. [Epub ahead of print] PubMed PMID: 31581906.
Shaĭdakov EV, Mel’tsova AZ, Porembskaia OI, Kudinova EA, Korzhevskiĭ DÉ, Kirik OV, Sukhorukova EG. [Experience with using cyanoacrylate glue in endovascular treatment of varicose veins]. Angiol Sosud Khir. 2017;23(4):62-67. Russian. PubMed PMID: 29240057.
Lam YL, De Maeseneer M, Lawson J, De Borst GJ, Boersma D. Expert review on the VenaSeal® system for endovenous cyanoacrylate adhesive ablation of incompetent saphenous trunks in patients with varicose veins. Expert Rev Med Devices. 2017 Oct;14(10):755-762. doi 10.1080/17434440.2017.1378093. Review. PubMed PMID: 28892412.
Lane TR, Kelleher D, Moore HM, Franklin IJ, Davies AH. Cyanoacrylate glue treats great saphenous vein incompetence in the anticoagulated patient. J Vasc Surg Venous Lymphat Disord. 2013 Jul;1(3):298-300. doi: 10.1016/j.jvsv.2012.09.007. Epub 2013 Feb 15. PubMed PMID: 26992590.
Lu PYJ, Fung CHC, Brooks C. Real-World Safety and Efficiency of Treating Symptomatic Varicose Veins with Endovenous Closure of Great, Small, and Anterior Accessory Veins Using Cyanoacrylate Glue (VenaSeal™): A Single-surgeon Multicenter Retrospective Study. Ann Vasc Surg. 2024 Dec 12;112:3-9. doi: 10.1016/j.avsg.2024.11.101. Epub ahead of print. PMID: 39672268.
Morrison N, Gibson K, McEnroe S, Goldman M, King T, Weiss R, Cher D, Jones A. Randomized trial comparing cyanoacrylate embolization and radiofrequency ablation for incompetent great saphenous veins (VeClose). J Vasc Surg. 2015 Apr;61(4):985-94. doi: 10.1016/j.jvs.2014.11.071. Epub 2015 Jan 31. PubMed PMID: 25650040.
Morrison N, Gibson K, Vasquez M, Weiss R, Jones A. Five-year extension study of patients from a randomized clinical trial (VeClose) comparing cyanoacrylate closure versus radiofrequency ablation for the treatment of incompetent great saphenous veins. J Vasc Surg Venous Lymphat Disord. 2020 Mar 20. PII: S2213-333X(20)30105-0. doi: 10.1016/j.jvsv.2019.12.080. [Epub ahead of print] PubMed PMID: 32205125.
O’Banion LA, Reynolds KB, Kochubey M, Cutler B, Tefera EA, Dirks R, Kiguchi MM. Treatment of superficial venous reflux in CEAP 6 patients: a comparison of cyanoacrylate glue and radiofrequency ablation techniques. J Vasc Surg Venous Lymphat Disord. 2021 Jan 13:S2213-333X(21)00001-9. doi: 10.1016/j.jvsv.2020.12.082. Epub ahead of print. PMID: 33453440.
Park I. Human Saphenous Vein Histopathology 2 Years After Cyanoacrylate Closure Using the VenaSeal™ System. Ann Vasc Surg. 2021 Feb;71:534.e17-534.e21. doi: 10.1016/j.avsg.2020.09.017. Epub 2020 Sep 16. PMID: 32949737.
Tang TY, Yap CJQ, Chan SL, Soon SXY, Yap HY, Lee SQW, Choke ETC, Chong TT. Early results of an Asian prospective multicenter VenaSeal real-world postmarket evaluation to investigate the efficacy and safety of cyanoacrylate endovenous ablation for varicose veins. J Vasc Surg Venous Lymphat Disord. 2021 Mar;9(2):335-345.e2. doi: 10.1016/j.jvsv.2020.03.020. Epub 2020 May 7. PMID: 32387378.
Watts TJ, Thursfield D, Haque R. Allergic contact dermatitis caused by VenaSeal tissue adhesive. Contact Dermatitis. 2019 Jun;80(6):393-395. doi 10.1111/cod.13206. Epub 2019 Jan 30. PubMed PMID: 30582174.
Wilczko J, Szary C, Plucinska D, Grzela T. Two-Year Follow-Up after Endovenous Closure with Short-Chain Cyanoacrylate versus Laser Ablation in Venous Insufficiency. J Clin Med. 2021 Feb 7;10(4):628. doi: 10.3390/jcm10040628. PMID: 33562190; PMCID: PMC7914451.
https://www.ajsccr.org/index.php
Zierau UT and Lahl W: Recurrence Discussion in Varicose Veins Therapy – A Critical Examination of the Vein Stump discussion; J. Vasc. Endovasc. Therapy 2019, Vol.4 No.2:13

